
PNU 리서치
- 메인으로 이동
- 연구/산학
- PNU 리서치
화학과 최정모(사진) 교수팀이 생체분자 응축제 연구에 활용할 수 있는 단순한 화학 모델 시스템 개발에 성공했다.
‘생체분자 응축체(biomolecular condensate)’는 세포 내에서 특정 생체분자가 국소적으로 조밀하게 분포하는 덩어리다. 신호 전달, 스트레스 반응, 유전자 발현 조절 등 다양한 생물학적 기능을 수행해 최근 신약 개발 및 질병 연구에서 중요한 주제로 부각되고 있다.
생체분자 응축체는 세포 내에서 생체분자들이 자발적으로 모여 형성되며, 다양한 종류가 알려져 있다. 세포가 스트레스를 받을 때 mRNA(메신저 리보핵산)와 단백질이 모여 일시적으로 단백질 합성을 조절하는 구조체인 ‘스트레스 과립(Stress granules)’이나 mRNA를 분해·저장하는 세포질 내 구조체인 ‘P-바디(P-bodies)’, 단백질 합성 장치인 리보솜을 만드는 ‘인(Nucleolus)’ 등이 모두 생체분자 응축제에 해당한다.
이들은 세포 내에서 여러 가지 기능을 수행할 수 있으며, 특히 생체분자의 국소적 농도가 높아지면서 효소 활성 등이 비약적으로 증대될 수 있다. 이에 따라 생체분자 응축체의 형성 원리를 탐구해 새로운 생체 촉매 플랫폼을 설계하려는 연구가 세계적으로 널리 시도되고 있다.
생체분자 응축체의 형성과 소멸은 기본적으로 ‘생체분자-생체분자’ 상호작용과 ‘생체분자-용매’ 상호작용의 경쟁에 의해 결정된다. 이번 연구에서는 이 두 가지 요소를 포함하는 가장 작은 모델 시스템을 만드는 데 성공했다.
연구팀은 간단한 화학 물질로 생체분자 응축제 모방에 나섰다. 세포 속 응축제와 비슷한 현상을 실험실에서 쉽게 구현할 수 있는 단순한 화학 시스템으로, ‘Fmoc’라는 특수한 화학 작용기를 결합시킨 아미노산을 사용했다.
* Fmoc(fluorenylmethoxycarbonyl) 작용기: 소수성을 띠고 있는 여러 고리 작용기로, 단백질의 말단을 보호하기 위한 용도로 활용된다.
이 화학 물질은, Fmoc 작용기는 물을 싫어해(소수성) 스스로 뭉치는 반면, 아미노산의 뼈대 부분은 물을 좋아하는 성질(친수성)을 갖고 있어 생체분자-용매 상호작용에 참여할 수 있다. 연구팀은 아미노산의 구조를 조금씩 바꾸며 어떤 조건에서 가장 잘 뭉치는지를 실험했다.
아미노산의 곁사슬을 변화시키면서 분자의 소수성 정도를 세밀하게 변화시킬 수 있었는데, 다양한 곁사슬을 도입해 생체분자 응축체가 시험관 내에서 형성되는지, 형성된다면 안정적으로 그 상태가 유지되는지를 살폈다. 그리고 이 모델 시스템을 이용해 실제로 포집된 분자의 촉매 활성이 증가함을 확인했다.
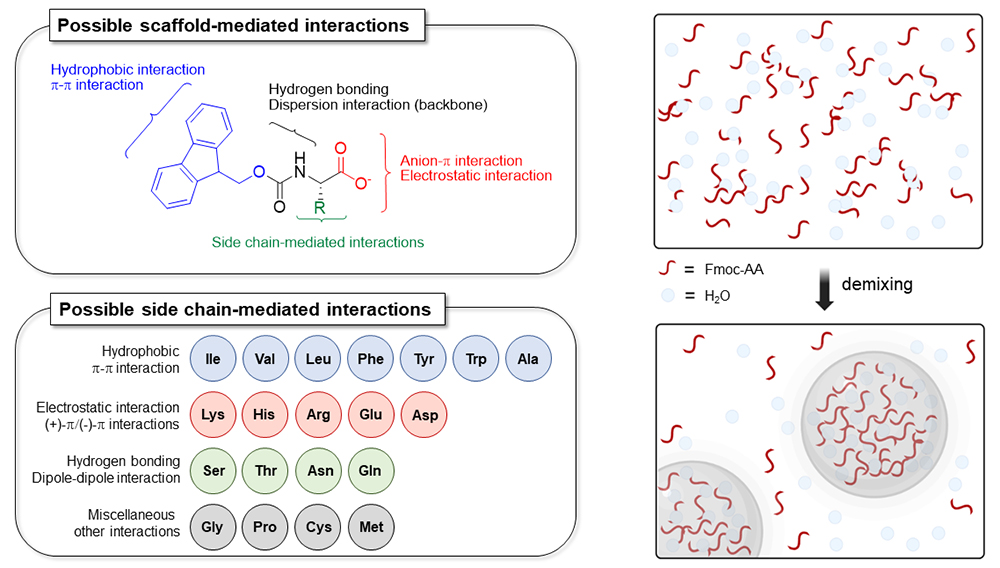
【액체-액체 상 분리를 만들어낼 수 있는 아미노산 유도체의 구조와 사용 가능한 곁사슬의 종류 및 액체-액체 상 분리 과정을 그린 모식도】
이번 연구는 부산대와 경희대 연구팀이 공동으로 수행했다. 경희대는 실험적 검증을, 부산대는 모델링을 담당했다. 부산대 연구팀은 분자동역학 시뮬레이션* 기법을 활용해 모델 분자가 응축체를 형성하는 화학적 기작을 분석했다. 특히 분자의 소수성 정도가 증가함에 따라 응축체 형성 경향성이 높아지는 것을 정량적으로 확인했으며, 이를 통해 이 모델 시스템에서는 소수성 상호작용이 응축체 형성의 주된 메커니즘임을 증명했다.
* 분자동역학(molecular dynamics) 시뮬레이션: 각 원자를 공처럼, 결합을 용수철처럼 취급하고 원자들이 주고받는 상호작용을 고려해 이들의 움직임을 시간에 따라 추적해 나가는 컴퓨터 시뮬레이션 기법.
생체분자 응축체의 형성 원리는 세포의 기능을 분자 차원에서 이해하는 데 반드시 필요한 개념이다. 이번 연구를 통해 생체분자 응축제의 형성 원리와 이렇게 만들어진 응축제 안에서 화학반응이 활발해지는 것을 확인했다.
최정모 교수는 “이번에 개발한 모델 시스템은 화학적으로 변화시키기 매우 용이하기 때문에 다양한 상호작용을 도입할 수 있고, 이를 이용해 생체분자 응축체의 형성 원리를 보다 깊이 있게 탐구할 수 있다. 이는 생명체의 기능에 밀접하게 연결돼 있으므로, 여기서 얻은 지식을 질병 치료 등에 활용할 수 있을 것”이라고 기대했다.
또한 이 시스템을 이용해 친수성 용매 내에 소수성 방울을 만들어 친수성 용매와 소수성 용매를 모두 필요로 하는 유기화학 반응 등도 진행할 수 있어 합성화학의 새로운 방법론으로의 응용도 전망된다.
한편, 이번 연구는 국제 학술지 『Biomacromolecules』 1월 26일자 온라인판에 게재됐다.
- 논문 제목: A Single Amino Acid Model for Hydrophobically Driven Liquid-Liquid Phase Separation(소수성 상호작용으로 추동되는 액체-액체 상 분리를 위한 단일 아미노산 모형)
- 논문 링크: https://doi.org/10.1021/acs.biomac.4c01410
해당 연구는 한국연구재단의 우수신진연구사업 지원을 받았다.
[Abstract]
The study presents a minimalistic model for liquid-liquid phase separation (LLPS) using fluorenylmethoxycarbonyl (Fmoc)-protected single amino acids (Fmoc-AAs). The authors systematically investigate how different Fmoc-AAs undergo LLPS based on hydrophobic interactions, pH, and ionic strength. Their findings highlight residue-dependent variations in critical concentrations and phase behavior, demonstrating that hydrophobic interactions predominantly drive phase separation. Furthermore, they explore the transition from liquid condensates to solid aggregates, revealing that this transformation may be governed by mechanisms distinct from LLPS. These insights contribute to the understanding of biomolecular condensation and its implications in cellular organization and protein aggregation diseases.
The researchers also analyze how environmental factors such as salt concentration, pH, and temperature affect the stability and behavior of Fmoc-AA condensates. Notably, the study shows that mixing different Fmoc-AAs, including enantiomers, significantly enhances the stability of condensates by disrupting molecular stacking, thereby preventing rapid aggregation. This suggests that phase separation and subsequent fibrillization are controlled by different molecular interactions. Additionally, molecular dynamics simulations corroborate these experimental observations, further elucidating the role of hydrophobicity in the condensation process.
Beyond fundamental insights, the study explores potential applications of Fmoc-AA condensates in mimicking cellular environments. The authors demonstrate that these condensates can selectively accommodate biomolecules and facilitate chemical reactions, highlighting their potential as artificial cells or catalytic microreactors. The enhanced reaction rates within the condensates suggest that they provide a unique microenvironment for biochemical transformations. Overall, this research advances our understanding of phase separation and protein aggregation, offering a versatile model system with applications in synthetic biology and material science.
- Author (Pusan National University): Jeong-Mo Choi (Department of Chemistry)
- Title of original paper: A Single Amino Acid Model for Hydrophobically Driven Liquid-Liquid Phase Separation
- Journal: Biomacromolecules
- Web Link: https://doi.org/10.1021/acs.biomac.4c01410
